20
20
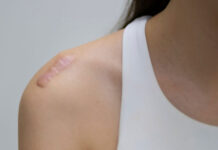
La dermatite atopica, malattia cronica della pelle, causa un prurito intenso e costante che si manifesta generalmente nei primi mesi di vita del bambino.
Di solito i trattamenti topici sono sufficienti ad alleviare il problema. Tuttavia, nei casi da moderati a severi è necessario ricorrere a trattamenti sistemici.
Trattamenti sistemici per dermatite atopica
Attualmente, i trattamenti sistemici disponibili per i bambini di età inferiore ai 6 anni con dermatite atopica moderata-severa non controllata con terapie topiche potrebbero non avere un’efficacia e una sicurezza ottimali.
Al contempo, il trattamento della dermatite atopica negli adulti e nei bambini di età superiore ai 6 anni in presenza di condizioni infiammatorie di tipo 2 avviene con il dupilumab.
Uno studio condotto da ricercatori britannici e statunitensi pubblicato su Lancet si è posto come obiettivo la valutazione di efficacia e sicurezza del dupilumab in abbinamento a corticosteroidi topici a bassa potenza proprio nei bambini di età compresa tra 6 mesi e 6 anni che presentavano una dermatite atopica di grado da moderato a severo.
Lo studio
Lo studio di fase III, randomizzato in doppio cieco e controllato con placebo, è stato condotto in 31 ospedali, cliniche e istituzioni accademiche in Europa e Nord America.
I pazienti arruolati avevano un’età compresa tra 6 mesi e 6 anni e presentavano dermatite atopica da moderata a grave, con un punteggio dell’Investigator’s Global Assessment (IGA) pari a 3-4, diagnosticata secondo i criteri di consenso dell’American Academy of Dermatology e una risposta inadeguata ai corticosteroidi topici.
I pazienti sono stati assegnati in modo casuale al gruppo placebo sottocutaneo ovvero al gruppo dupilumab, somministrato in modo differente in base al peso del bambino: 200 mg con peso da 5 a 15 kg, 300 mg con peso compreso tra 15 e 30 kg. La somministrazione avveniva a cadenza quadrisettimanale, abbinata a corticosteroidi topici a bassa potenza per 16 settimane.
Gli obiettivi
Lo studio si era prefisso come endpoint primario alla sedicesima settimana il raggiungimento di una percentuale di pazienti che presentassero un punteggio IGA pari a 0-1, corrispondente a pelle chiara o quasi chiara.
L’endpoint secondario chiave (endpoint comprimario per il mercato UE) alla settimana 16 era dato da una percentuale di pazienti che presentassero un miglioramento dell’Eczema Area and Severity Index di almeno il 75% rispetto al basale (EASI-75).
Dupilumab e dermatite atopica: i risultati
Lo studio ha arruolato 162 soggetti, assegnati in modo casuale al gruppo dupilumab, nel numero di 83, o placebo associato a corticosteroidi topici, 79.
Alla sedicesima settimana è stato evidenziato che un numero superiore di pazienti trattati con dupilumab rispetto a placebo presentava un IGA pari a 0-1, con un rapporto di 23 a 3 e un EASI75 con un rapporto di 44 a 8.
La prevalenza complessiva degli eventi avversi è stata simile nel gruppo dupilumab (53 [64%] di 83 pazienti) e nel gruppo placebo (58 [74%] di 78 pazienti).
L’incidenza di congiuntivite è stata maggiore nel gruppo dupilumab (quattro) rispetto al gruppo placebo (nessuno). Nessun evento avverso correlato a dupilumab è stato grave o ha portato all’interruzione del trattamento.
Dupilumab ha migliorato significativamente i segni e i sintomi della dermatite atopica rispetto al placebo nei bambini di età inferiore ai 6 anni.
Il farmaco è stato dunque ben tollerato e ha mostrato un profilo di sicurezza accettabile, simile ai risultati ottenuti nei bambini più grandi e negli adulti.
A. S. Paller, E. L. Simpson, E. C. Siegfried et al., Dupilumab in children aged 6 months to younger than 6 years with uncontrolled atopic dermatitis: a randomised, double-blind, placebo-controlled, phase 3 trial, Lancet, 2022 Sep 17;400(10356):908-919. Doi: 10.1016/S0140-6736(22)01539-2.